Superoksididismutaasi

Superoksididismutaasi eli SOD on entsyymi, joka katalysoi superoksidi-ionien disproportioitumista vetyperoksidiksi ja hapeksi. Superoksididismutaasi on tärkeä antioksidantti useissa soluissa ja sitä esiintyy lähes kaikissa esitumallisissa ja aitotumaisissa. Superoksididismutaasin EC-numero on EC 1.15.1.1.[1]
Rakenne ja toiminta
[muokkaa | muokkaa wikitekstiä]Superoksidisdismutaasia esiintyy lähes kaikissa eliöissä. Aito- ja esitumaisten superoksididismutaasit poikkeavat toisistaan kofaktorina toimivien metallikationien suhteen. Aitotumaisilla eliöillä superoksididismutaasi vaatii yleensä toimiakseen sekä kupari- että sinkki-ionin, kun esitumaisilla kofaktorina on tyypillisesti rauta- tai mangaani-ioni. Eräillä Streptomyces-suvun bakteereilla kofaktorina toimii nikkeli-ioni.[2]
Useimmilla aitotumaisilla superdismutaasista on kaksi muunnosta: superoksididismutaasi 1 ja superoksididismutaasi 2. Superoksididismutaasi 1 esiintyy sytoplasmassa ja on rakenteeltaan dimeeri ja siihen sitoutuvat sinkki- ja kupari-ionit. Superoksididismutaasi 2 on mitokondrioissa esiintyvä muoto, joka on rakenteeltaan tetrameeri ja sitoutunut mangaani-ioneihin. Nisäkkäillä on myös superoksididismutaasi 3, joka on superoksididismutaasi 2:n tavoin tetrameeri, mutta jonka rakenteeseen on sitoutunut kupari -ja sinkki-ioneja. Superoksididismutaasi 3 esiintyy soluväliaineessa.[3]
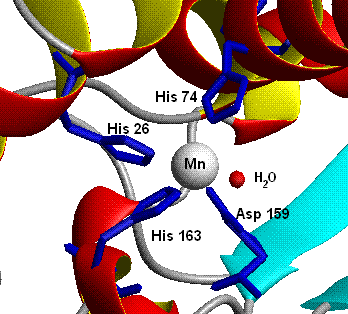
Superoksididismutaasi hajottaa superoksidi-ionin kahdessa vaiheessa. Ensimmäisessä vaiheessa superoksidi-ioni muodostaa entsyymin ja entsyymiin sitoutuneen siirtymämetallikationin kanssa kompleksin ja hapettuu hapeksi. Tällöin metallikationi pelkistyy. Kupari pelkistyy hapetusluvulta +II hapetusluvulle +I ja mangaani tai rauta pelkistyy hapetusluvulta +III hapetusluvulle +II. Superoksidi-ioni kykenee hapettamaan metallikationit niiden alkuperäiselle hapetusluvulle pelkistyen itse vetyperoksidiksi.[3][4] Superoksididismutaasin toimintaa voidaan kuvata seuraavilla reaktioyhtälöillä.
- M(n+1)+-SOD + O2- → Mn+-SOD + O2
- Mn+-SOD + O2-; + 2H+ → M(n+1)+-SOD + H2O2.
Superoksididismutaasia inhiboi muun muassa syanidi-ioni[1].
Lähteet
[muokkaa | muokkaa wikitekstiä]- ↑ a b EC 3.4.15.1 - peptidyl-dipeptidase A BRENDA. Viitattu 25.11.2012. (englanniksi)
- ↑ Stanley Falkow, Eugene Rosenberg, Karl-Heinz Schleifer, Erko Stackebrandt: The procaryotes, s. 97. Springer, 2006. ISBN 978-0-387-25492-0 Kirja Googlen teoshaussa (viitattu 07.12.2012). (englanniksi)
- ↑ a b Liza A. Pon,Eric A. Schon: Methods in Cell Biology: Mitochondria, s. 381. Academic Press, 2007. ISBN 978-0-12-544173-5 Kirja Googlen teoshaussa (viitattu 07.12.2012). (englanniksi)
- ↑ Ivano Bertini: Biological Inorganic Chemistry, s. 333. University Science Books, 2007. ISBN 978-1-891389-43-6 Kirja Googlen teoshaussa (viitattu 07.12.2012). (englanniksi)